Testiculaire kanker is de meest voorkomende maligniteit bij mannen in de leeftijd van 25 tot 45 jaar. Hij is over het algemeen te behandelen. Daarom kunnen de meeste patiënten worden genezen. Om testiculaire kanker in een vroeg stadium te kunnen detecteren, moeten alle mannen uit de puberteit hun testikels periodiek scannen. Ontdek alles wat belangrijk is over dit onderwerp: hoe kun je zaadbalkanker herkennen? Wat veroorzaakt hem? Welke behandelingsopties zijn er? Wat zijn de kansen op genezing van zaadbalkanker?

Snel overzicht
- Wat is zaadbalkanker? Kwaadaardige tumor van het testiculaire weefsel. Meestal wordt slechts één zaadbal aangetast. De meest voorkomende vormen van zaadbalkanker zijn zogenaamde seminomen, gevolgd door niet-seminomen.
- frequentie: Meest voorkomende kanker bij mannen tussen 25 en 45 jaar (mediane leeftijd van patiënten: 38 jaar) – Testiculaire kanker is goed voor 20 tot 30 procent van alle kankers in deze leeftijdsgroep. Jongere en oudere mannen worden minder vaak ziek. Over het algemeen is testiculaire kanker een zeldzame kanker (ongeveer 4.000 nieuwe gevallen in Duitsland per jaar).
- symptomen: tastbare, pijnloze verharding in het scrotum, vergrote testikels (met zwaarte), vergrote, pijnlijke borsten, in gevorderde stadia extra symptomen als gevolg van secundaire tumoren (metastasen) zoals hoesten en pijn op de borst in longmetastasen
- behandeling: Verwijdering van de aangetaste zaadbal; daarna, afhankelijk van het tumorstadium en testiculaire kanker vorm monitoring strategie (“wachten en kijken”), chemotherapie of radiotherapie; mogelijk verwijdering van aangetaste lymfeklieren
- voorspelling: Testiculaire kanker is over het algemeen zeer behandelbaar. De meeste patiënten kunnen worden genezen.
Testiculaire kanker: symptomen en vroege detectie
Hetzelfde geldt voor testiculaire kanker (testiculair carcinoom) als voor andere soorten kanker: hoe eerder de kwaadaardige tumor wordt ontdekt en behandeld, hoe groter de kans op herstel. Maar hoe herken je zaadbalkanker?
Tastbare verharding
Een van de meest voorkomende symptomen van zaadbalkanker is een pijnloze verharding in het scrotum: het oppervlak van de zaadbal voelt nodulair of tuberculair aan. Elke man kan zelfs een harde knoop in zijn testikels (mogelijk testiculaire kanker) voelen als hij zichzelf regelmatig onderzoekt. Het is belangrijk om de gemodificeerde testikels te vergelijken met de tweede testikels. Dat komt omdat verschillen beter kunnen worden gedetecteerd.
In ongeveer 95 procent van alle gevallen treft testiculaire kanker slechts een van de twee testikels. Bij de resterende vijf procent van de patiënten ontwikkelen kankercellen zich in beide testes.
Toename in omvang en zwaarte
Als een testis groter wordt, is dit ook een mogelijk teken van zaadbalkanker. De meeste patiënten melden dit symptoom de eerste keer dat ze naar de dokter gaan. Deze toename in grootte kan te wijten zijn aan de tumorgroei zelf. Aan de andere kant kan de reden een ophoping van vloeistof zijn (hydrocele of waterbreuk).
Door het vergroten van de omvang van de aangetaste testikels voelt dit moeilijk. deze zwaarte gaat met sommige patiënten mee pull die kan uitstralen in de lies.
pijn
Bij sommige patiënten zijn Pijn in het gebied van de zaadbal meer symptomen van testiculaire kanker. Bloeden in het kankerweefsel kan prikken of knijpen veroorzaken. Pijn is echter zelden het eerste teken van zaadbalkanker.
Bij pijn in het gebied van de zaadbal moet men niet onmiddellijk denken aan zaadbalkanker! Meestal is het een testiculaire ontsteking (orchitis) of epididymitis (epididymitis) erachter. Een onderzoek bij de uroloog geeft zekerheid.
Bij geavanceerde testiculaire kanker nemen de lymfeklieren in de achterste buikholte toe. Dat kan rugpijn veroorzaken.
borstgroei
Sommige testiculaire tumoren produceren vrouwelijke hormonen. Bij sommige patiënten kunnen bijvoorbeeld verhoogde niveaus van oestrogeen in het bloed worden gedetecteerd. Het zwangerschapshormoon beta-humaan choriongonadotropine (β-HCG) wordt ook geproduceerd door sommige testiculaire tumoren. Als gevolg van de hormoonproductie vergroot de borst van het mannetje (een of beide zijden). Artsen praten erover met dit testiculaire kankersymptoom echte gynaecomastieomdat het klierweefsel in de borst hier echt prolifereert. Gynaecomastie daarentegen beschrijft een borstgroei veroorzaakt door vetafzetting.
De β-HCG wordt ook beschouwd als een belangrijke tumormarker. Dit is een bloedbeeld dat typisch is voor sommige testiculaire kankers. Het helpt om testiculaire kanker te diagnosticeren en om het verloop van de ziekte te beoordelen.
De vergrote borsten kunnen ook pijn.
Symptomen als gevolg van kolonies van kanker
Als testiculaire kanker vordert, kunnen kankercellen zich via lymfatische en bloedvaten door het lichaam verspreiden en ergens nieuwe tumoren vormen. Dergelijke dislocaties (metastasen) van zaadbalkanker treden op voornamelijk in de longen op. Maar het kan ook andere organen beïnvloeden, zoals de hersenen, botten en lever. Afhankelijk van het aangetaste orgaan treden overeenkomstige klachten op.
Longmetastasen veroorzaken bijvoorbeeld vaak hoesten (soms met bloederig sputum) en kortademigheid. Zelfs pijn op de borst zijn dan veel voorkomende symptomen. Testiculaire kankerachtige laesies in de botten veroorzaken botpijn. Levermetastasen kunnen onder andere merkbaar worden door misselijkheid, verlies van eetlust en ongewenst gewichtsverlies. Als kankercellen in de hersenen zich verspreiden, kunnen neurologische tekorten worden toegevoegd aan de gemeenschappelijke symptomen van testiculaire kanker.
Testiculaire kanker: behandeling
In principe zijn de volgende behandelingsmaatregelen beschikbaar voor de testiculaire kankertherapie:
- operatie
- Bewakingsstrategie: “afwachten”
- Radiotherapie (straling)
- chemotherapie
De behandelend arts zal een aangepast behandelplan voorstellen aan een patiënt met testiculaire kanker. Patiënten moeten de arts vragen deel te nemen aan het project “Second opinion testiculaire tumoren” (www.zm-hodentumor.de) om deel te nemen. In dit op internet gebaseerde project kunnen artsen testiculaire kankerspecialisten vragen om een tweede beoordeling van de bevindingen van de patiënt en de geplande therapie. Dit kan de planning van de therapie aanzienlijk verbeteren, indien nodig.
De eerste stap van de behandeling van zaadbalkanker is meestal een operatie. De verdere behandelingsstappen zijn afhankelijk van het stadium van de ziekte en het type tumor (seminoom of niet-seminoom – veruit de meest voorkomende vormen van zaadbalkanker).
Testiculaire kanker: chirurgie
Bij testiculaire kankerchirurgie worden de aangetaste testes, epididymis en zaadstreng chirurgisch verwijderd. Artsen spreken van de Ablatorio testis of orchiectomy, In enkele gevallen kan een zaadbalkanker ook worden geopereerd zodat een deel van de zaadbal behouden blijft. Dit kan dan hormonen blijven produceren. Deze procedure is vooral nuttig voor patiënten die slechts één zaadbal hebben. Voor de zekerheid moeten de geopereerde testes meestal achteraf worden bestraald.
Op verzoek van de patiënt kan tijdens de procedure een weefselmonster ter grootte van een korrel worden genomen van de andere testikel en direct onder de microscoop worden onderzocht. Dit is raadzaam omdat bij ongeveer vijf procent van de patiënten, ook in de tweede zaadbal, pathologisch veranderde cellen kunnen worden gevonden. In dit geval kan deze zaadbal mitentfernt hetzelfde zijn.
De testikel op afstand kan op verzoek van de patiënt door een prothese worden vervangen. Voor dit doel wordt een siliconenkussen in de juiste maat en vorm in het resterende scrotum gebruikt. Als chemotherapie nodig is nadat de testikels zijn verwijderd, moet de testiculaire prothese nog worden gebruikt.
tumorstadia
Het verwijderde testiculaire kankerweefsel wordt histologisch onderzocht. Samen met andere onderzoeken (zoals computertomografie) is het mogelijk om het stadium van de ziekte te bepalen (zie hieronder: onderzoeken en diagnose). Er zijn grofweg verschillende tumorstadia:
- Stadium I: kwaadaardige tumor alleen in de zaadbal, geen metastasen.
- Fase II: besmetting van aangrenzende (regionale) lymfeklieren, maar geen kankerachtige laesies op afstand (metastasen op afstand); Afhankelijk van de grootte of het aantal aangetaste lymfeklieren wordt stadium II verder onderverdeeld (IIA, IIB, IIC).
- Stadium III: ook aanwezige metastasen op afstand (zoals in de longen); afhankelijk van de ernst verdere onderverdeling (IIIA, IIIB, IIIC).
seminoom
de meest voorkomende vorm van zaadbalkanker is het seminoom. In het vroege stadium (stadium I) is de verdere behandeling na het verwijderen van de zaadbal vaak beperkt tot de monitoring van de strategie: De patiënt moet regelmatig nagaan of de kanker is teruggekeerd. In eerste instantie zijn deze vervolgonderzoeken zeer nauw gepland. Later kunnen de tijdsintervallen daartussen worden vergroot.
Om de prognose te verbeteren, kan men na de operatie ook een vroeg stadiumseminoom hebben Chemo- of radiotherapie traktatie. Als het seminoom al vergevorderd is op het moment dat de testikels worden verwijderd, krijgen patiënten in alle gevallen chemotherapie of radiotherapie. Welke vorm van therapie in een individueel geval de beste optie is, hangt onder andere af van het exacte tumorstadium.
In principe is het ook mogelijk om radiotherapie en chemotherapie te combineren. Deze therapievariant wordt momenteel getest in klinische studies in een seminoom.
Lees meer over de behandeling van seminomen en andere belangrijke informatie over deze meest voorkomende vorm van zaadbalkanker in het artikel Seminom.
nonseminoma
Niet-seminomen zijn de tweede meest voorkomende vorm van zaadbalkanker na seminomen. Ook hier zijn de behandelingsstappen na het verwijderen van de zaadbal afhankelijk van het tumorstadium:
Testiculaire kanker fase I
In dit vroege stadium bij niet-seminomen (zoals in seminomen) na het verwijderen van de zaadbal is meestal voldoende monitoring van de strategie uit: met behulp van regelmatige controles kunnen mogelijke terugvallen worden gedetecteerd en vroeg worden behandeld.
Per definitie is testiculaire kanker beperkt tot de testikels in stadium I en heeft zich nog niet verspreid naar lymfeklieren of andere lichaamsgebieden. Dit kan echter niet met 100% zekerheid worden gezegd, ondanks moderne beeldvormingstechnieken zoals computertomografie. Soms zijn kankeruitzaaiingen zo klein dat ze niet worden gedetecteerd in beeldvorming. Twee factoren kunnen wijzen op dergelijke onzichtbare (occulte) metastasen:
- Bij het onderzoeken van het geëxtraheerde tumorweefsel is gebleken dat de zaadbalkanker in aangrenzende lymfoïde of bloedvaten is gebroken. Het risico op occulte metastasen neemt dan toe tot ongeveer vijftig procent.
- Na tumorverwijdering vallen de respectieve tumormarkers in het bloed niet af of stijgen zelfs niet.
In dergelijke gevallen is er een verhoogd risico dat de zaadbalkanker zich al heeft verspreid. Voor de veiligheid is dan na het verwijderen van de zaadbal geen bewakingsstrategie, maar een chemotherapie (1 cyclus) aanbevolen: patiënten ontvangen gedurende drie dagen drie chemotherapeutica: cisplatine, etoposide en bleomycine (samen kortweg PEB genoemd). Het kan ook raadzaam zijn om de lymfeklieren in de achterste buik te verwijderen (lymphadenectomy). Vervolgens wordt de betrokken persoon nauwlettend gevolgd en gecontroleerd.
Testiculaire kankerstadia IIA en IIB
In deze twee stadia van testiculaire kanker zijn lymfeklieren al aangetast en dus vergroot. Dan zijn er twee opties voor de verdere behandeling na het verwijderen van de zaadbal:
- Ofwel de geteisterde Lymfeklieren operatief verwijderd, mogelijk gevolgd door een chemotherapie (als individuele kankercellen in het lichaam moeten blijven).
- Of de patiënt ontvangt onmiddellijk na de testiculaire operatie drie cycli van chemotherapie, Daarna kunt u nog steeds worden getroffen Verwijder operatief lymfeklieren.
Testiculaire kanker stadia IIC en III
In deze gevorderde niet-vrouwelijke fasen zullen patiënten de testiculaire verwijdering volgen drie tot vier chemotherapiecycli behandeld. Als er nog steeds aangetaste lymfeklieren zijn, worden deze verwijderd (lymphadenectomy).
Bijwerkingen van testiculaire kankertherapie
de chemotherapie Testiculaire kanker (en andere vormen van kanker) kunnen een aantal bijwerkingen hebben: de medicijnen (cytotoxische medicijnen) zijn zeer giftig voor cellen – niet alleen voor de testiculaire kankercellen, maar ook voor gezonde lichaamscellen zoals bloedplaatjes, bloedcellen en haarwortelcellen. Mogelijke bijwerkingen zijn daarom bijvoorbeeld bloedarmoede, bloeding, haaruitval, misselijkheid en braken, verlies van eetlust, ontsteking van de slijmvliezen, gehoorstoornissen en ongemak op de handen en voeten. Cytostatische medicijnen vallen ook het immuunsysteem aan. Patiënten zijn daarom gevoeliger voor ziekteverwekkers tijdens de behandeling.
In de regel verdwijnen deze bijwerkingen na het voltooien van chemotherapie. Bovendien kunnen artsen helpen met passende maatregelen en tips om de ongewenste effecten van de behandeling (zoals misselijkheid) te verlichten.
Bij een (vermoedelijke) betrokkenheid van de lymfeklieren in de achterste buik is dit gebied vaak met een radiotherapie behandeld. De meest voorkomende bijwerking hier is milde misselijkheid. Het komt enkele uren na de straling voor en kan met medicijnen worden verlicht. Andere mogelijke bijwerkingen zijn voorbijgaande diarree en huidirritatie in het te behandelen gebied (zoals roodheid, jeuk).
Testiculaire kanker: oorzaken en risicofactoren
Testiculaire kanker (testiculair carcinoom) bij volwassen mannen wordt in meer dan 90 procent van de geslachtscellen in de testes aangetroffen. Zij zullen Kiemceltumoren (kiemtumoren) genoemd. De kleine rest wel niet-germinale tumoren out. Ze ontstaan uit ondersteunend en bindweefsel van de zaadbal.
Kiemceltumoren: seminomen en niet-seminomen
De kiemceltumoren zijn verdeeld in twee hoofdgroepen: de seminomen en de niet-seminomen.
een seminoom is het resultaat van gedegenereerde spermastamcellen (spermatogonia). Het is de meest voorkomende vorm van kwaadaardige kiemceltumor in de testikels. De gemiddelde leeftijd van de patiënten is ongeveer 40 jaar.
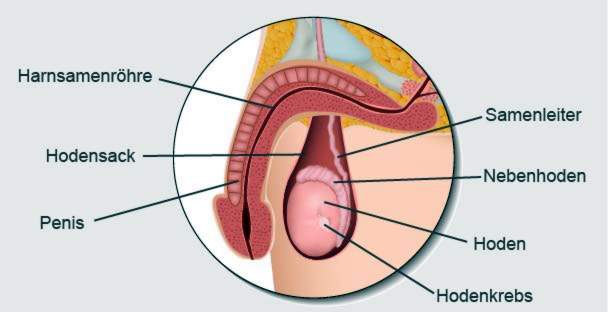
De term nonseminoma omvat alle andere vormen van zaadbalkanker die voortkomen uit andere weefseltypen. Zij omvatten:
- Dooierzak tumor
- choriocarcinoma
- embryonaal carcinoom
- Teratoma of de kwaadaardige vorm teratocarcinoma
Patiënten met een niet-seminoom zijn gemiddeld 25 jaar oud.
De voorloper van seminomen en niet-minderjarigen zal zijn testiculaire intraepitheliale neoplasie (TIN) genoemd (intraepitheliaal = gelokaliseerd in het bedekkende weefsel, neoplasie = neoplasma). De neoplasmata zijn afkomstig van embryonale kiemcellen vóór de geboorte. Ze rusten in de teelballen en kunnen zich later ontwikkelen tot zaadbalkanker.
Niet-germinale tumoren
Veel zeldzamer dan de kiemceltumoren zijn de niet-kiemtumoren (kiemtumoren, gonadale stromatumoren). Dit zijn celproliferaties die ontstaan uit de ondersteunende en bindweefselcellen van de zaadbal. Ze zijn goedaardig of kwaadaardig. De belangrijkste vertegenwoordiger van kwaadaardige kiemtumoren is de Leydigcel teelbalkanker, Hij komt uit de Leydig-cellen. Ze produceren het geslachtshormoon testosteron en stimuleren zo de spermaproductie.
Niet-germinale tumoren komen vooral voor bij kinderen. Bij volwassen mannen zijn ze zeer zeldzaam (waarschijnlijk op oudere leeftijd).
Waarom ontstaat zaadbalkanker?
De exacte oorzaak van zaadbalkanker is nog niet bekend. Onderzoekers hebben in het verleden echter enkele risicofactoren geïdentificeerd voor de ontwikkeling ervan.
Voormalige testiculaire kankerziekte
Een eerdere testiculaire kankerziekte is de belangrijkste risicofactor: iedereen die testiculaire kanker heeft gehad, heeft een 30-voudig verhoogd risico om opnieuw een kwaadaardige testiculaire tumor te ontwikkelen.
ingedaalde testikels
Normaal migreren de twee testikels vanuit de buikholte naar het scrotum tijdens de ontwikkeling van de foetus (soms zelfs na de geboorte). Aan de andere kant blijft één testikel op één testikelhoogte (Maldescensus-testis) of beide testikels blijven in de buikholte of in de lies (testikels in de buik of de lies). Soms kunnen de testikels worden gevonden bij de ingang van de testikels en kunnen ze onder druk in het scrotum worden geduwd, maar schuiven ze onmiddellijk terug. Dan spreekt men van glijdend hoefijzer.
Een niet-ingedaalde zaadbal verhoogt de kans op het ontwikkelen van zaadbalkanker. Dit risico bestaat nog steeds, zelfs wanneer de niet-ingedaalde testikels chirurgisch zijn gecorrigeerd: het testiculaire kankerrisico is dus 2,75- tot 8-voudig hoger in geopereerde hoge hoogte dan in een normaal testiculair systeem. In het bijzonder hangt in de glijdende horsetode het risico van degeneratie af van de duur van de afwijking. Boven het scrotum is de lichaamstemperatuur bij 35 tot 37 graden Celsius aanzienlijk hoger dan in het scrotum (ongeveer 33 graden Celsius). De hogere temperatuur kan het testiculaire weefsel beschadigen. Daarom is het risico op testiculaire kanker verhoogd bij (eerdere) niet-ingedaalde testikels.
Verkeerde bevestiging van de urethra-mond
Als de mond van de urethra zich onder de eikel bevindt (dwz aan de onderkant van de penis), spreken artsen van hypospadie. Studies suggereren dat het risico op zaadbalkanker wordt verhoogd door deze miskraam.
Hypospadie en niet-ingedaalde testikels lijken een soortgelijke genetische oorzaak te hebben. Ze komen daarom vaak samen. Ze kunnen echter ook afzonderlijk voorkomen.
Genetische factoren
Studies hebben ook aangetoond dat erfelijke factoren waarschijnlijk de ontwikkeling van zaadbalkanker beïnvloeden. Omdat in sommige families dezelfde tumor vaak voorkomt. Getroffen broers hebben ook een tot twaalfvoudig verhoogd risico op het ontwikkelen van zaadbalkanker. Zelfs zonen van zieke vaders hebben statistisch gezien meer kans om testiculair carcinoom te ontwikkelen dan zonen van gezonde vaders.
Bovendien is gebleken dat zaadbalkanker veel vaker voorkomt bij mannen met een lichte huid in Europa dan bij in Afrika geboren mannen.
Overmaat oestrogeen tijdens de zwangerschap
Veruit de meest voorkomende vorm van testiculaire kanker (kiemceltumoren) komt voort uit een voorloper genaamd TIN (testiculaire intra-epitheliale neoplasie). Het is gebaseerd op kiemcellen die zich vóór de geboorte in het embryo ontwikkelen. Een van de redenen hiervoor is hormonale onbalans tijdens de zwangerschap, meer bepaald een teveel aan vrouwelijke hormonen (oestrogenen). Dit kan hoogstwaarschijnlijk de ontwikkeling van de testis van het ongeboren kind verstoren en leiden tot het precancereuze TIN.
Er wordt bijvoorbeeld een lichte overmaat oestrogeen waargenomen bij zwangere vrouwen die het eerste kind of een tweeling verwachten of ouder dan 30 jaar. Het gebruik van geneesmiddelen met oestrogenen kan de hormoonspiegels bij zwangere vrouwen verhogen. Zwangere vrouwen worden tegenwoordig echter nauwelijks behandeld met hormonen.
onvruchtbaarheid
Zelfs met een man die niet in staat is om de zaadbalkanker te produceren, wordt het risico verhoogd. Onvruchtbaarheid is gebaseerd op onderontwikkelde testes (hypogonadisme) of op een tekort of volledige afwezigheid van sperma in de zaadvloeistof (oligospermie of azoöspermie).
De oorzaken van onvruchtbaarheid kunnen verschillen. Soms is het het gevolg van een orchitis veroorzaakt door het bofvirus. Zelfs afwijkingen (afwijkingen) in het genoom kunnen mannen onvruchtbaar maken, bijvoorbeeld het Klinefelter-syndroom.
Externe invloeden
Wereldwijd is het aantal zaadbalkankerziekten de afgelopen 20 jaar aanzienlijk toegenomen. Experts vermoeden daarom dat externe invloeden in de kindertijd en vroege volwassenheid ook de ontwikkeling van kanker bevorderen. Maar dat moet nader worden onderzocht.
Testiculaire kanker: diagnose en onderzoek
Mannen moeten regelmatig hun eigen testikels onderzoeken en voelen, vooral tussen de 20 en 40 jaar. Iedereen die een verandering in het scrotum diagnosticeert, moet snel een uroloog raadplegen. Deze specialist in urinewegen en geslachtsorganen kan het vermoeden van zaadbalkanker ophelderen door middel van een paar onderzoeken.
Arts-patiënt gesprek
Eerst praat de arts in detail met de patiënt om zijn medische geschiedenis te verhogen (anamnese). De arts vraagt naar eventuele symptomen, bijvoorbeeld:
- Heb je een verharding in het scrotum opgemerkt?
- Voelt u een gevoel van zwaarte op de genoemde plaats of zelfs pijn?
- Heb je andere veranderingen aan je opgemerkt, zoals een toename van de borstgrootte?
In het gesprek zal de arts ook mogelijke risicofactoren verduidelijken: Heb je in het verleden een testiculaire tumor gehad? Had je een niet-ingedaalde zaadbal? Heeft iemand in uw familie last van zaadbalkanker? Elk stukje informatie is belangrijk, zelfs die die voor de patiënt onbeduidend lijken. Zwelling in de lies, rugpijn of hoest kan bijvoorbeeld wijzen op kankerafzettingen (metastasen) en dus op een gevorderde zaadbalkanker.
Palperende testikels
Het anamnese-interview wordt gevolgd door een lichamelijk onderzoek. Vooral de bimanueel onderzoek van de testikels is belangrijk. Daarbij houdt de arts de zaadbal stevig vast met één hand en scant deze met de andere hand op onregelmatigheden. Op deze manier worden beide testikels zorgvuldig onderzocht, ook al verandert er maar één verdachte. De sitevergelijking kan belangrijke informatie opleveren (zaadbalkanker beïnvloedt meestal slechts één zaadbal alleen). Wanneer palpatieonderzoek van toepassing is: Elke vergroting of verharding in en op de testes is vermoedelijk tumor.
Tip: elke man moet regelmatig zijn eigen testikels voelen. Zodat hij verdachte veranderingen vroegtijdig kan detecteren en een arts kan raadplegen. Als het echt testiculaire kanker is, verbetert een vroege diagnose de kansen op herstel!
Hoe verder te gaan in het zelfonderzoek van de zaadbal, leest u in de testikels.
Palpatie van de borst
Als onderdeel van het lichamelijk onderzoek van de arts wordt ook verdacht van testiculaire kanker in de borst van de man. De vrouwelijke hormonen geproduceerd door een testiculaire tumor veroorzaken dat de borstklieren pijnlijk opzwellen.
ultrageluid
Het echografisch onderzoek voor de diagnose van zaadbalkanker wordt uitgevoerd met een sonde met hoge resolutie. Typisch zijn onregelmatige gebieden die donkerder lijken dan het omringende weefsel. Zelfs kleinere en niet-voelbare testiculaire kanker foci kunnen worden gedetecteerd in de echografie. Het onderzoek wordt op beide testes uitgevoerd om een bilaterale besmetting uit te kunnen sluiten.
bloedonderzoek
Als testiculaire kanker wordt vermoed, is een uitgebreid onderzoek van het bloed ook belangrijk. De arts wint het voor een verwijzing naar de Algemene staat van de patiënt en op de Functie van individuele organen, Aan de andere kant, de zogenaamde tumormarkers in het bloed. Dit zijn eiwitten die alleen detecteerbaar zijn in het geval van kanker of worden geproduceerd in kankerpatiënten in opvallend verhoogde hoeveelheden.
Een van die tumormarkers bij zaadbalkanker is de alfa-fetoproteïne (AFP), Dit eiwit wordt tijdens de zwangerschap geproduceerd in de dooierzak van een ongeboren kind. Bij volwassenen wordt het alleen in zeer kleine hoeveelheden lever- en darmcellen geproduceerd. Als een man een verhoogde AFP-waarde heeft, duidt dit op testiculaire kanker – vooral bepaalde vormen van niet-seminomen (dooierzaktumor en embryonaal carcinoom). Voor een seminoom daarentegen is de AFP-waarde normaal.
Een andere belangrijke tumormarker bij zaadbalkanker is de beta-humaan choriongonadotrofine (β-HCG), De waarde ervan is vooral verhoogd in choriocarcinoom (een vorm van niet-seminoom), in een seminoom, echter alleen in ongeveer 20 procent van alle gevallen.
de Lactaat dehydrogenase (LDH) is een enzym dat ook in veel lichaamscellen voorkomt. Het is alleen geschikt als complementaire tumormarker (naast AFP en β-HCG) bij zaadbalkanker.
De bloedwaarde van placentale alkalische fosfatase (PLAP) is vooral verhoogd bij een seminoom. Omdat de waarde ook bij bijna alle rokers wordt verhoogd, is PLAP slechts zeer beperkt als tumormarker bij zaadbalkanker.
Deze tumormarkers zijn niet bij elke testiculaire kankerpatiënt verhoogd. Omgekeerd kunnen gezonde personen ook verhoogde waarden hebben. De tumormarkers alleen staan daarom geen betrouwbare diagnose toe. Maar ze zijn geschikt om het verloop van een testiculaire kankerziekte te beoordelen. Als bijvoorbeeld de tumormarkers na een voltooide behandeling weer stijgen, kan dit een terugval aangeven (recidief).
CT en MRI
Als de diagnose van testiculaire kanker wordt bevestigd, biedt computertomografie (CT) informatie over de verspreiding van de tumor: röntgenfoto’s worden gebruikt om gedetailleerde dwarsdoorsnedebeelden te produceren van de bekken-, buik- en borstholten en mogelijk het hoofd. Bovendien zijn vergrote lymfeklieren en testiculaire metastasen (dislocaties van de tumor in andere delen van het lichaam) over het algemeen gemakkelijk te herkennen. Gewoonlijk wordt de patiënt voorafgaand aan onderzoek geïnjecteerd met een contrastmiddel om beeldvorming te verbeteren.
Een alternatief voor CT is MRI (Magnetic Resonance Imaging, MRI): het biedt ook gedetailleerde dwarsdoorsneden van het inwendige van het lichaam, zij het met behulp van magnetische velden (geen röntgenstralen). De patiënt wordt daarom niet blootgesteld aan straling. Een MRI wordt bijvoorbeeld uitgevoerd als de patiënt allergisch is voor het contrastmiddel dat bij CT moet worden gebruikt.
Blootstelling van de zaadbal
Om een testiculaire kankerdiagnose te garanderen, wordt de vermoedelijke testis chirurgisch blootgesteld. De arts herkent dan meestal met het blote oog of er een kwaadaardige testiculaire tumor bestaat. Bij twijfel neemt hij een weefselmonster dat tijdens de procedure op kankercellen wordt onderzocht. Als dit het geval is, wordt gecontroleerd of het Seminom of niet-Seminom is. In het geval van zaadbalkanker wordt de aangetaste testis onmiddellijk verwijderd.
Testiculaire kanker: ziekteverloop en prognose
Testiculaire kanker kan meestal goed worden behandeld en meestal ook worden genezen. Vijf jaar na een diagnose testiculaire kanker nog steeds ongeveer 96 procent van de patiënten (5-jaars overleving).
Deze goede prognose is voornamelijk te wijten aan het feit dat bij de meeste patiënten het testiculair carcinoom in een vroeg stadium wordt ontdekt. De kansen op succes van de behandeling zijn dan groot. Als de kanker zich echter al heeft verspreid op het moment van diagnose, vergroot dit de kansen op herstel. De prognose in individuele gevallen wordt echter ook beïnvloed door bijvoorbeeld …
- welk type tumor aanwezig is (seminomen hebben over het algemeen een gunstiger prognose dan niet-seminomen)
- hoe goed de patiënt op de therapie reageert
- waar metastasen zich al in het lichaam hebben gevormd (voor metastasen van lymfeklieren en long is de prognose meestal gunstiger dan voor metastasen in lever, bot of hoofd)
- hoe lang na de laatste chemotherapie duurt totdat de kanker weer vordert (hoe langer, hoe goedkoper)
- welke meetwaarden de tumormarkers hebben
Bullet vruchtbaarheid
Veel patiënten zijn bang voor de behandeling van zaadbalkanker kaal worden of geen seksueel verlangen om meer te voelen. Meestal kan de behandelend arts de getroffenen echter kalmeren: de meerderheid van de patiënten heeft ze alleen unilaterale zaadbalkanker, Dan hoeven alleen de zieke testikels te worden verwijderd. De resterende testikels zijn meestal voldoende om seksualiteit en vruchtbaarheid te behouden. De zaadproductie kan nadien echter enigszins worden aangetast. Bovendien zijn er mannen bij wie de zaadproductie zelfs vóór de ziekte en de behandeling is aangetast.
Wat nog belangrijker is, zijn de kwesties vruchtbaarheid en seksuele publicatie vooral voor de (enkele) patiënten die minderjarig zijn bilaterale testiculaire kanker lijden of aan een eerdere ziekte al een zaadbal verloren, De operatie probeert dan alleen kwaadaardig veranderd tumorweefsel te verwijderen en zoveel mogelijk testiculair weefsel te verkrijgen. Als het echter nodig is om beide testikels (of de enige bestaande testikels) volledig te verwijderen, kan de getroffen persoon niet langer kinderen produceren. Het geslachtshormoon testosteron wordt niet langer geproduceerd. De afwezigheid ervan vermindert het seksuele verlangen en de erectiele functie.
Kortom, alle patiënten met zaadbalkanker vóór het begin van de behandeling aanbevolen, uw eigen Onderzoek vruchtbaarheid te laten. Dit kan het beste worden gedaan door een monster ejaculatie in het laboratorium te analyseren op het aantal, de vorm en het drijfvermogen van het sperma (spermaanalyse). Als alternatief kan men ook de bloed-FSH (follikelstimulerend hormoon) meten: als het wordt verhoogd, kan dit wijzen op een verminderde spermaproductie.
Ook moeten patiënten met testiculaire kanker vóór het begin van de behandeling overwegen of ze veilig zijn Vries sperma in willen vertrekken (cryopreservatie). Dit zal later kunstmatige inseminatie mogelijk maken als de patiënt van nature niet in staat is om te reproduceren na de behandeling van testiculaire kanker. Voor het conserveren (350, – tot 650, – Euro) en opslag (200, – tot 450, – Euro per jaar) moet u meestal zelf betalen.
Tip: Patiënten moeten vooraf persoonlijk vragen bij hun eigen ziekteverzekering, als dit niet de kosten overneemt. Soms maken kassa’s een uitzondering.
Dit na een operatie aan de zaadbalkanker testosteron ontbreekt kan worden vervangen door spuiten, tabletten, gelpreparaten of pleisters.
Testiculaire kanker: terugval
Om een mogelijke terugval van testiculaire kanker (recidief) in een vroeg stadium te kunnen detecteren, worden met succes behandelde patiënten regelmatig onderzocht. In het begin zijn de controles erg strak. Later worden de tijdsintervallen tussen beide langer. Dit is vooral het geval wanneer er geen symptomen zijn en geen tekenen van een mogelijke terugval.
De waarschijnlijkheid van een recidief van zaadbalkanker hangt met name af van Tumorfase bij de eerste diagnose en van de Type eerste behandeling uit. Als testiculaire kanker bijvoorbeeld alleen in de vroege fase na de operatie wordt gevolgd (surveillancestrategie), is het risico op terugval groter dan bij chemotherapie na de ingreep.
Als het gaat om een terugval, meestal binnen de eerste twee tot drie jaar na de eerste behandeling. Latere recidieven zijn zeldzamer. Die Patienten erhalten dann eine sogenannte Salvage-Chemotherapie: Das ist eine hochdosierte Chemotherapie. Sie ist viel wirksamer als eine normal dosierte Chemotherapie, wie sie normalerweise in der Erstbehandlung von Hodenkrebs angewendet wird. Dafür hat sie schwerere Nebenwirkungen. Unter anderem werden das Knochenmark und damit die Blutbildung bei der Hochdosis-Therapie viel starker geschädigt. Deshalb werden den Patienten meist blutbildende Stammzellen übertragen (Stammzelltransplantation):
Die Patienten bekommen zuerst eine normal dosierte Chemotherapie, um möglichst viele Krebszellen abzutöten. Dann verabreicht man ihnen Wachstumsfaktoren, welche die Blutbildung anregen. So entstehen ausreichend Stammzellen, die sich aus dem Blut des Patienten herausfiltern lassen. Nach der hochdosierten Chemotherapie (Salvage-Chemotherapie) werden den Patienten dann die entnommenen Blutstammzellen wieder über eine Vene zurückgegeben. Die Stammzellen siedeln sich im geschädigten Kncohenmark an und beginnen, neue Blutzellen zu produzieren.
Insgesamt gilt: Ein Rückfall ist bei Hodenkrebs eher selten. Auf die dann verabreichte Hochdosis-Chemotherapie sprechen 50 bis 70 Prozent der Patienten günstig an.
Weiterführende Informationen
Selbsthilfegruppe:
- Deutsche Krebsgesellschaft